
Výukové materiály ZŠ Kaplice, Školní 226

Roztok = rozpuštěná látka + rozpouštědlo
Zastoupení jednotlivých složek v roztoku označujeme jako koncentrace roztoku.
Koncentraci roztoku udává nejčastěji:Př. Procenta složky roztoku:
- Hmotnostní zlomek (hmotnostní procentová koncentrace)
- Objemový zlomek (objemová procentní koncentrace)
- Molární koncentrace (látková koncentrace)
- Normální koncentrace
- 8% ocet:
100 častí roztoku = 8 častí kyselina octová + 92 častí voda
100g roztoku = 8 g kyselina octová + 92g voda
- 3% peroxid vodíku
100 častí roztoku = 3 častí kyselina octová + 97 častí voda
100g roztoku = 3 g kyselina octová + 97g voda
Hmotnostní zlomek w(s) rozpuštěné látky s v roztoku je podíl hmotnosti m(s) rozpuštěné látky s a hmotnosti m roztoku.
w(s) - hmotnostní zlomek látky (složky) rozpuštěné v roztoku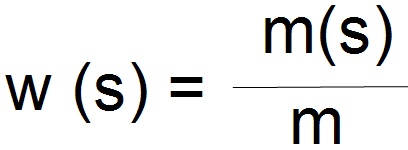
m(s) - hmotnost látky (složky) rozpuštěné v roztoku
m - hmotnost roztoku
Vyjadřuje se nejčastěji v procentech a udává tedy počet gramů rozpuštěné látky ve 100 g roztoku.
Hmotnostní zlomky se převádějí na procenta vynásobením 100.
a) např. w(kyseliny octové)= 8/100 = 0,08, tj. 8% ocet
b) např. w(peroxid vodíku) = 3/100 = 0,03, tj. 3% peroxid vodíku
Podle hodnoty w(s) roztoky jsou:
- koncentrované - mají vetší w(s) než zředěné
- zředěné