
Výukové materiály ZŠ Kaplice, Školní 226

prvky |
soustava |
vazba |
látek |
příklady |
|---|
Chemické prvky byly uspořádány do tabulky periodické soustavy podle vzrůstajícího protonového čísla a podle elektronů ve valenční vrstvě - D. I. Mendělejevem
Periodický zákon
- vlastnosti prvků a jejich sloučenin se periodicky mění v závislosti na protonovém čísle
- prvky ve stejné hlavní skupině mají stejný počet valenčních elektronů, a tudíž mají podobné vlastnosti
Rozdělení periodické tabulky
- 7 vodorovných řad - periody (č. periody = počet elektronových vrstev)
- 18 svislých sloupců (16 skupin)
- hlavní I. A - VIII. A (č. skupiny = počet valenčních elektronů)
- vedlejší I. B - VIII. B
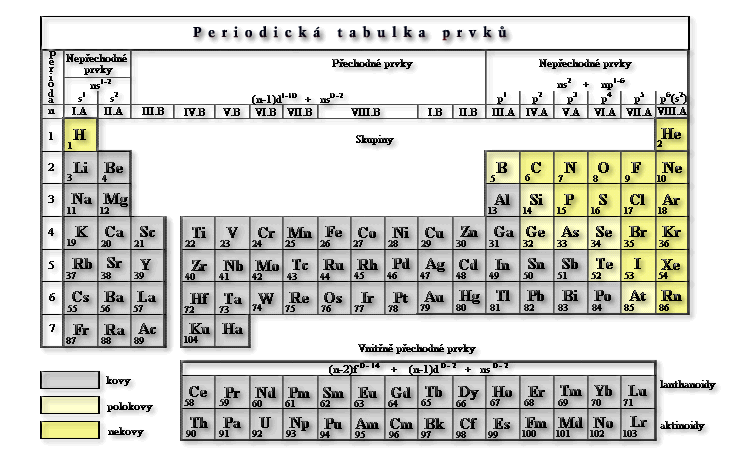
obr. Animovaná chemie - CD
Dělení prvků podle fyzikálních vlastností
Podle původu
- Přirozené
- plynné: H2, N2, O2, F2, Cl2, vzácné plyny
- kapalné: Br2, Hg
- pevné: ostatní (především kovy)
- Připravené umělé
- plutonium (94), americium (95), curium (96), berkelium (97), californium (98), einsteinium (99), fermium (100)
Podle fyzikálních vlastností
- kovy: Na, Au, Zn, K, Ca, Al
- nekovy: N2, H2, He, Cl2
- polokovy: Ge, Si
Některé skupiny prvků mají své skupinové názvy
- I.A - alkalické kovy (kromě vodíku)
- II.A - kovy alkalických zemin
- VI.A - chalkogeny
- VII.A - halogeny
- VIII.A - vzácné (inertní) plyny